今天上午(7月30日),NMPA官网发布了《2019年度药品审评报告》(下称《报告》)。《报告》显示,2019年,药审中心受理新注册申请8082件(含器械组合产品5件),其中需技术审评的注册申请6199件(含4907件需药审中心技术审评和行政审批的注册申请),直接行政审批(无需技术审评)的注册申请1878件。
在颇受关注的1类创新药方面,药审中心共受理注册申请共700件(319个品种),品种数较2018年增长了20.8%。其中,受理1类创新药的新药临床试验(IND)申请302个品种,较2018年增长了26.4%;受理1类创新药的新药上市申请(NDA)17个品种,较2018年减少了8个品种。
在国产1类创新药方面,药审中心共受理注册申请528件(244个品种),其中受理临床申请503件(228个品种),上市申请25件(16个品种)。按药品类型统计,化学药401件(144个品种),生物制品127件(100个品种),创新药的适应症主要集中在抗肿瘤、抗感染和消化系统疾病领域。
一、药品注册申请受理情况
2019年,药审中心受理新注册申请8082件(含器械组合产品5件,以受理号计,下同),其中需技术审评的注册申请6199件(含4907件需药审中心技术审评和行政审批的注册申请),直接行政审批(无需技术审评,下同)的注册申请1878件。
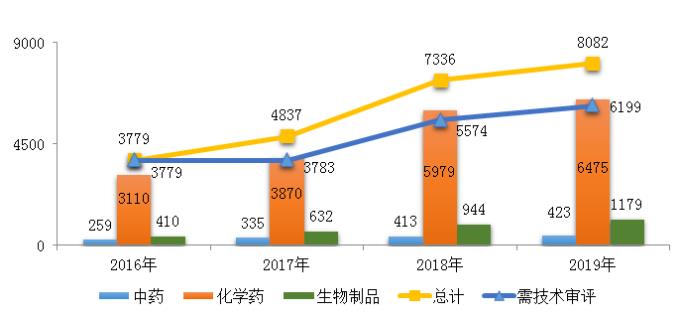
药审中心受理的8077件药品注册申请中,化学药注册申请受理量为6475件,占2019年全部注册申请受理量的80.2%,2016-2019年各类药品注册申请受理情况详见图1。
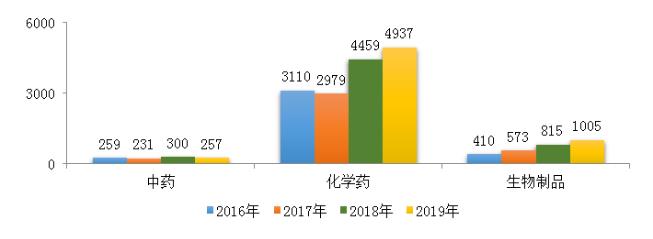
图1 2016-2019年各类药品注册申请受理情况注:1.2019年受理量中含5件器械组合产品的注册申请,故上图中2019年受理注册申请总量大于中药、化学药、生物制品受理注册申请之和;2. 药审中心的直接行政审批工作自2017年开始,所以2016年无直接行政审批注册申请,所有受理注册申请均需技术审评。图2 2017-2019年需技术审评的各类药品注册申请受理情况
2019年,受理需技术审评的注册申请6199件,较2018年增加11.21%,其中化学药注册申请为4937件,较2018年增长了10.72%,占全部需技术审评的注册申请受理量的79.64%;中药注册申请257件,较2018年降低了14.33%;生物制品注册申请1005件,较2018年增长了23.3%。2016-2019年需技术审评的化学药、中药和生物制品注册申请受理情况详见图2。
药审中心受理1类创新药注册申请共700件(319个品种),(化学药的品种数以活性成分统计,中药和生物制品的品种数均以药品通用名称统计,下同),品种数较2018年增长了20.8%。其中,受理1类创新药的新药临床试验(IND)申请302个品种,较2018年增长了26.4%;受理1类创新药的新药上市申请(NDA)17个品种,较2018年减少了8个品种。
药审中心受理国产1类创新药注册申请528件(244个品种),其中受理临床申请503件(228个品种),上市申请25件(16个品种)。按药品类型统计,化学药401件(144个品种),生物制品127件(100个品种),创新药的适应症主要集中在抗肿瘤、抗感染和消化系统疾病领域。
药审中心受理5.1类化学药进口原研药注册申请157件(92个品种),受理1类进口创新药注册申请172件(75个品种),创新药的适应症主要集中在抗肿瘤、内分泌和神经系统疾病领域。
详情请点击http://www.nmpa.gov.cn/WS04/CL2168/379010.html